当・分子硬組織生物学分野では,悪性腫瘍の発症・進展メカニズムの解析を行っております。大きく分けて以下の3つのテーマで解析を展開しています。
- 間葉系細胞由来悪性腫瘍・骨肉腫の発症と転移機構の解析
- 舌がんの発症と悪性化機構の解析
- 天然化合物由来の新規抗腫瘍薬の検索
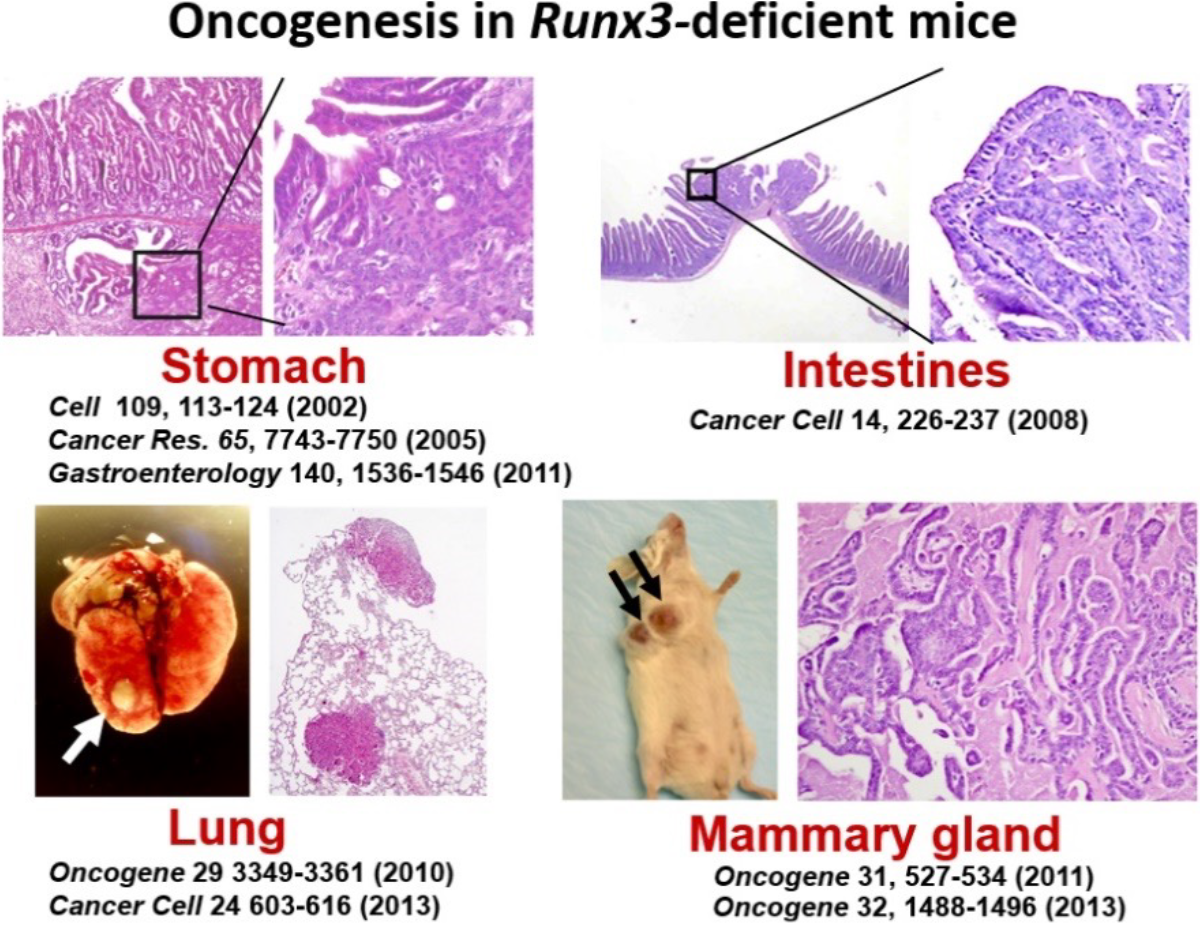
これまで私たちは,一貫して転写因子RUNXの機能解析を推進してきました。RUNXファミリー遺伝子(RUNX1, 2,3)は,「がん遺伝子」あるいは「がん抑制遺伝子」として機能することが知られています。特にRUNX3は、私たちが世界で初めてRunx3ノックアウトマウスを作出し,消化器がんとの因果関係を明らかにして以降(Cell, 109, 113-124, 2002; Cancer Res., 65, 7743-7750, 2005; Gastroenterology, 140, 1536-1546, 2011; Cancer Cell, 14, 226-237, 2008),ほぼすべてのヒトがんにおいて,その機能的な関与が報告されてきました。
Runx3遺伝子欠損マウスは,消化器がんのみならず,肺がんや乳がんも高頻度に発症します。Runx3は「がん抑制遺伝子」として,広く悪性腫瘍の発症に関与します。
最近になって私たちは,骨肉腫(およびT細胞リンパ腫)の解析から,ヒトがんにおける最も普遍的な「がん抑制遺伝子」p53が不活性化された状況下においては,Runxファミリー遺伝子が,最も強力な「がん遺伝子」Mycの発現を強く誘導することを見出しました(Oncogene 41, 683-691, 2022; Gene 819, 146234, 2022)。すなわち,p53非存在下では,RUNX転写因子は「がん遺伝子」として機能すると考えられます。
これらの成果を踏まえ,現在は骨肉腫のみならず,歯科学領域における最も重要な悪性腫瘍である「舌がん」の発症と悪性化機序の解析も,マウスモデルを構築して開始しています。
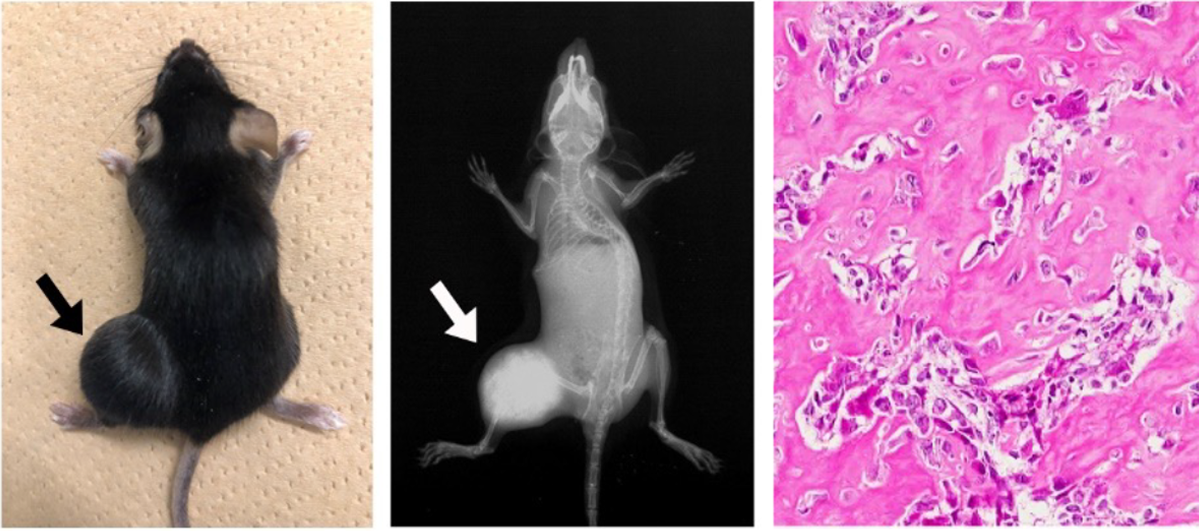
p53遺伝子を欠損させると,ヒト骨肉腫と性状が酷似した骨肉腫が発症します。この骨肉腫では,Runx遺伝子の発現が上昇し,それに伴い,過剰なMycの発現が観察されます。
p53非存在下でのみ「がん遺伝子」として機能するRUNXは,抗腫瘍ターゲットとして大変魅力的です。そこで,その効果的で特異的な阻害剤の検索を,
長崎大学海洋微生物抽出物ライブラリー 
を用いて実施しています。天然化合物由来の副作用の小さな抗腫瘍剤を同定し,その臨床応用をめざします。